
蔡尚,九三学社西湖大学支社主委,博士,西湖大学生命科学学院副院长,博士生导师,长江特聘教授。研究方向为干细胞的再生、谱系分化以及疾病状态下的功能异常。在Cell、Science和Cell Stem Cell等学术期刊发表多项研究成果。
《晏子春秋》有云,橘生淮南则为橘,生于淮北则为枳——同一棵橘树生长在淮河以南,结出的果实甘甜多汁;可要是移栽到淮河以北,同样的树种,却会长出又小又苦、无法食用的枳子,这不是因为橘树本身发生变化,而是生长的位置不同,让同一植物的功能发生了根本性反转。
两千多年前的自然哲思,竟在今天的肿瘤微观世界里得到了印证。
2022年,西湖大学/西湖实验室蔡尚团队首次证实乳腺癌细胞内藏着“胞内菌”是乳腺癌转移的重要帮凶,时隔4年,团队再登Cell。北京时间2026年2月4日,蔡尚团队在Cell发表题为“Divergent Tumor Immunity Determined by Bacteria-Cancer cell Engagement”的研究成果,系统揭示了瘤内菌差异化调控肿瘤免疫的双重作用。
肿瘤中的细菌正如这橘树——在肿瘤细胞外的细菌,能够诱导具有抗肿瘤功能的中性粒细胞亚群,激活免疫应答,进而抑制肿瘤复发,成了激活免疫的“甜橘”;而在肿瘤细胞内的细菌却变成抑制免疫的“苦枳”,可通过激活癌细胞自身的cGAS–STING–IL17B信号通路,诱导中性粒细胞进入免疫抑制状态,从而塑造免疫抑制性微环境,促进转移灶的长期存活与复发。
这场微观世界的“橘枳之变”,究竟是如何发生的?

论文截图
论文链接:https://www.cell.com/cell/fulltext/S0092-8674(25)01493-X

免疫舞台上的“冰与火之歌”
在肿瘤这个战场上,免疫系统有着截然不同的姿态,有的地方“烽火连天”,有的地方却一片静寂,这是由于免疫细胞的浸润和活性不同导致的。
根据这个特征,肿瘤可分为“热肿瘤”(免疫激活型)与“冷肿瘤”(免疫抑制型)。
“热肿瘤”环境中,免疫细胞全副武装,积极作战,密集浸润在肿瘤周围,患者对免疫治疗敏感,患者预后更好;
与“热肿瘤”相反,“冷肿瘤”的微环境中免疫系统“消极抵抗”,免疫细胞浸润较少,免疫应答受抑制,患者对免疫治疗不敏感。
这便是肿瘤的“冷”与“热”,一场在免疫舞台上演的“冰与火之歌”。
造成这两种状态的原因是什么?这涉及肿瘤微环境中多种因素的协同作用,包括物理屏障(如硬度)、化学信号(如酸碱度,氧环境)以及基质细胞间的复杂互作。尤其当肿瘤发生转移时,转移的肿瘤细胞必须适应新环境并调控局部免疫状态,从而实现生存与复发。
肿瘤细胞如何调控转移灶的免疫“冷”“热”特性,已成为肿瘤研究的重要议题。长久以来,科学家们始终困惑:为什么有些肿瘤天生是“冷肿瘤”?转移后的肿瘤又是如何精准“屏蔽”免疫系统的?
近年来肿瘤内存在细菌这一发现,给科学家带来全新的研究视角。
过去,大家普遍觉得肿瘤是癌细胞的“专属地盘”,但后来发现,肿瘤里还常驻着细菌,这个发现让科学家们开始从细菌的视角重新看待肿瘤和免疫系统的关系。相关研究表明,肿瘤内的细菌不是单纯“旁观者”,而是通过代谢产物、细菌组分或分泌蛋白等方式,直接或间接地影响癌细胞行为与免疫细胞功能,从而在特定条件下激活或抑制免疫系统。
尽管,科学家已经意识到瘤内菌的重要性,但是关于其机制还有许多秘密——这些细菌是怎么跑到肿瘤内的,怎么找到自己的专属位置?分布的位置不同,会不会导致不同的肿瘤免疫反应?
细菌生“南北”,作用各不同
在前期“胞内菌促转移”的研究基础上,蔡尚团队进一步关注肿瘤细胞的细菌在转移复发阶段的作用,这些肿瘤细胞内的细菌,是否会通过重塑远端转移灶的免疫环境,影响术后复发风险?
研究第一步,建立严格的胞内菌研究模型。
瘤内菌分“胞内”和“胞外”两种形式,要单独研究胞内菌的作用,首先得解决“如何只留胞内菌、清除胞外菌”的技术难题。
研究团队巧妙地构建了体外类器官-细菌共培养系统,引入特异清除胞外菌的抗生素(无法穿透细胞膜,能精准杀死胞外菌,却不会伤害肿瘤细胞内的细菌),彻底排除了胞外菌的干扰,实现了严格的胞内菌类器官模型。
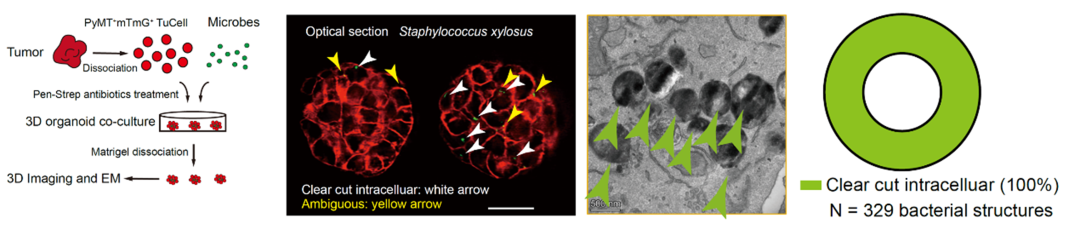
接下来,为了验证胞内菌与肿瘤复发的关系,团队做了两组关键小鼠实验。胞内菌类器官模型尾静脉回输的肿瘤复发实验显示,胞内菌的存在是肿瘤长期复发的关键因素,抗生素清除胞内菌可以有效降低乳腺癌肺部复发,复发率65%降到6.7%;临床前的小鼠乳腺癌术后复发模型显示,肺转移灶中细菌入侵信号越强,免疫抑制越明显,复发率也越高(达80%);而清除胞内菌后,复发率降至20%。
更关键的是,在没有免疫系统的小鼠身上,这种“胞内菌促复发”的效应几乎消失,说明胞内菌不是直接促进肿瘤生长,而是通过“操控免疫系统”间接影响肿瘤复发。

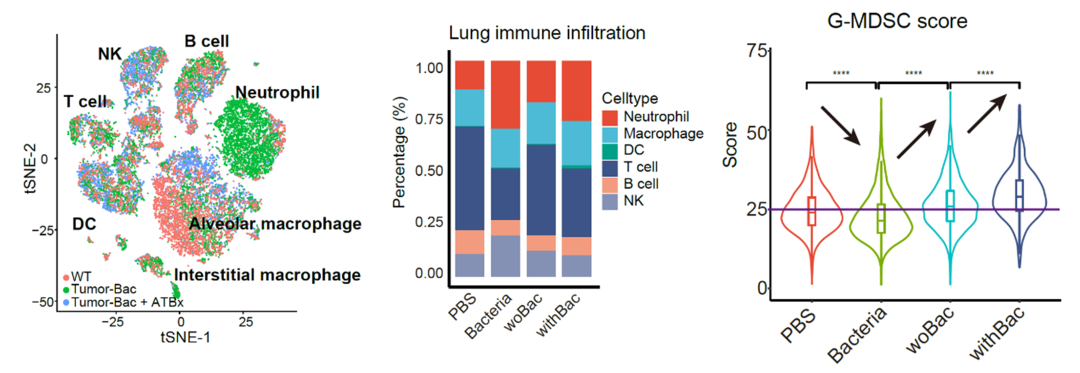
为什么胞内菌会抑制免疫反应?团队用单细胞RNA测序技术,对比了胞内菌和胞外菌对免疫细胞的影响,发现了他们的核心差异——
这两类细菌都会让中性粒细胞在肺部富集,但胞内菌诱导的中性粒细胞,会抑制免疫反应,类似髓源抑制性细胞;胞外菌诱导的中性粒细胞,基因表达偏向抗感染、抗肿瘤方向,能主动召唤其他免疫细胞一起攻击癌细胞。
简单说,胞内菌把免疫“友军”策反了,而胞外菌则让“友军”战斗力拉满。
知其然知其所然,胞内菌究竟是如何让中性粒细胞发生“叛变”的呢?
研究团队在对比携带和不携带胞内菌的肿瘤细胞后,发现胞内菌会激活一条关键信号通路:cGAS–STING–IL-17B。进一步实验证实,只有活的胞内菌才能触发这个通路,它们会让肿瘤细胞内累积双链DNA,激活cGAS–STING通路,进而诱导肿瘤细胞分泌IL-17B。
而IL-17B就是重要的“策反信号”,它是让中性粒细胞发生“叛变”的关键。如果通过基因敲除或药物阻断cGAS、STING或IL-17B中的任何一个环节,抑制型中性粒细胞会减少,T细胞可以恢复功能,肿瘤复发也会被显著抑制。
胞内菌可以激活肿瘤细胞内的STING通路,通过IL-17B让中性粒细胞“叛变”,抑制免疫,促进复发;胞外菌则无法激活肿瘤细胞的STING通路,直接诱导中性粒细胞变成“抗癌战士”,激活免疫,抑制复发。

细菌位置能调控肿瘤免疫反应的结论在小鼠身上得到了验证,为了能够真正落地到癌症治疗上,研究团队还继续做了人源验证——
从乳腺癌患者肿瘤组织中分离出以表皮葡萄球菌等为代表的肿瘤相关细菌,与人乳腺癌细胞共培养,发现STING和IL-17通路同样被激活;
用健康志愿者的中性粒细胞与“被细菌入侵的肿瘤细胞”一起培养,发现中性粒细胞会变成抑制型;如果直接添加重组人IL-17B,不用细菌也能诱导出同样效果,说明IL-17B在人源系统中亦具有保守的免疫调控作用;
分析大型乳腺癌患者队列数据,发现细菌入侵信号强、STING和IL-17通路活跃的患者,预后明显更差,这意味着“肿瘤胞内菌–中性粒细胞–免疫逃逸”的链路,在人类身上同样存在。
被忽视的细菌
或许能成为抗癌的新突破
从前期揭示“肿瘤胞内菌增强乳腺癌转移定植”,到本次阐明“肿瘤胞内菌、胞外菌差异化重塑中性粒细胞功能、调控转移复发免疫逃逸”,蔡尚课题组围绕乳腺癌肿瘤菌群,系统解析了其在肿瘤细胞力学适应和免疫调控两个层面的关键作用。
这项研究表明,相关细菌并非简单的“伴随菌群”,而是在特定空间定位和信号背景下,能够显著影响转移定植和免疫逃逸结局的重要生物学因素。瘤内菌的致病能力不仅与菌种相关,同时也与具体菌株的入侵能力息息相关。
细菌,一种单细胞生物体,在所有生物中数量最多,功能各异,是许多疾病传播的病原体,但同时也可以被人类利用制作酸奶、抗生素、处理废水等。
当在不同的场景,细菌的功能和角色便有了天翻地覆的变化。
在肿瘤内亦是如此。
在看到乳腺癌细胞内藏的“胞内菌”是乳腺癌转移的重要帮凶后,我们想到的办法或许是消灭细菌,但是在看到细菌的位置影响肿瘤的免疫后,我们开始反思,细菌或许可以不被消灭,而是调控它们的生长位置和作用方式,让免疫战场重新“燃”起来。
或许,我们可以开发能高效穿透肿瘤细胞膜的“靶向抗生素”,专门杀死躲在细胞内的胞内菌,从源头切断免疫抑制的“信号源”;
或许,我们还可以针对cGAS–STING–IL-17B这条核心信号通路,开发专门的抑制剂,让中性粒细胞不“叛变”;
再或许,我们可以输入胞外菌的安全组分,诱导中性粒细胞“抗癌战士”,让肿瘤由“冷”变“热”……
“橘生淮南则为橘,生于淮北则为枳”的千年哲思,最终在一场跨越十载的科学探索中,照进了肿瘤研究的微观世界。这一切的起点,源于十多年前的一次意外发现。
彼时还是斯坦福大学博士后的蔡尚,在构建小鼠乳腺癌模型时,意外发现不需要敲除某个具体的基因,只需要加入诱导剂(一种抗生素),肿瘤的转移就会受到影响。这个发现令他惊叹。
十年前,他偶然在文献里看到“抗生素可能影响肿瘤进展”的报道时,博后期间的发现突然又在脑海里清晰起来,或许肿瘤内真的存在细菌?
四年前,他们在Cell发文,首次证实乳腺癌组织中存在多种独特的“胞内菌”,并揭示它们在肿瘤转移定植过程中所起的关键作用。当时,他曾说,这项成果只是在乳腺癌研究领域开了一扇小窗,至于窗外的风景如何,期待有更多人一起眺望。
他和团队也是眺望人群中的一员,这一次,他们看见了更精彩的风景,看见了肿瘤细菌的位置与细节,生命的复杂与精妙。
科学的突破从来不只是偶然的幸运,谁也无法预料,灵光一闪的种子,在敏锐、勇气、坚持的浇灌下,会结什么样的果,开什么样的花,或许,这就是科学最动人的模样。
(来源:西湖大学WestlakeUniversity)